№6|2010
ПРОБЛЕМЫ, ПЕРСПЕКТИВЫ
bbk 000000
УДК 628.1.036:543.3
Особенности измерения цветности подземных вод Западно-Сибирского региона
Аннотация
Приведены результаты экспериментальных исследований по определению цветности подземных вод Западно-Сибирского региона, отобранных с глубины 80–200 м, с использованием методики измерения цветности, рекомендованной ГОСТ Р 52769-2007. Трудности определения цветности связаны с особенностями химического состава подземных вод и обусловлены образованием устойчивых коллоидных частиц, состоящих из Fe(OH)3 и растворенных органических веществ гумусового происхождения. Установлено, что цветность подземных вод в основном определяется присутствием коллоидных соединений железа и характеризуется как «кажущаяся» цветность воды.
Ключевые слова:
питьевая вода , подземные воды , цветность , водоподготовка , запах , вкус , коллоидные частицы , гумус
Скачать статью в журнальной верстке PDF
Органолептические показатели воды – цветность, запах и вкус – являются определяющими при оценке ее качества. Цветность служит индикатором пригодности воды для использования в питьевых целях, относится к физико-химическим показателям свойств природной и питьевой воды и характеризует количество содержащихся в ней окрашенных растворенных веществ. Измерение цветности природных вод необходимо для правильного выбора технологии водоподготовки. Согласно данным [1; 2], цветность природной воды обусловлена присутствием главным образом гуминовых и фульвокислот, связанных с гумусом почвы. В работах [3; 4] отмечается, что на цветность воды влияет присутствие соединений железа и других металлов в виде естественных примесей.
В международном стандарте ИСО для описания окраски воды используется термин «цвет». Получаемый в присутствии нерастворенного взвешенного вещества, он характеризуется как «кажущийся». Для аналитических целей представляет интерес «истинный цвет пробы». Он характеризуется как цвет, обусловленный растворенными веществами [5].
В России, в соответствии с ГОСТ Р 52769-2007, этот органолептический показатель характеризуется термином «цветность воды» и определяется двумя методами: визуально – для ориентировочной оценки цветности и фотометрически – для количественной оценки, с использованием хромокобальтовой или платинокобальтовой шкалы в качестве калибровки. Визуальный и фотометрический методы можно применять отдельно или в сочетании. Однако даже сочетание этих методов не исключает неточности в определении цветности воды, если цвет пробы будет отличаться от эталонов сравнения. Особую трудность представляют подземные воды. В методиках определения цветности в соответствии с ГОСТ Р 52769-2007 не учитываются особенности подземных вод, что может приводить к ошибкам и получению недостоверных результатов. На примере подземных источников Западно-Сибирского региона рассмотрим некоторые проблемы, возникающие при определении цветности.
Несмотря на обилие в Западной Сибири рек, озер и водохранилищ, для питьевого водоснабжения часто используют подземные воды [6; 7]. Содержание примесей в них разнообразно как по качественному составу, так и по количественному соотношению. Основной примесью, влияющей на качество подземных вод указанного региона, являются соединения железа. Обогащение подземных вод этими соединениями происходит вследствие выщелачивания и растворения железистых минералов и пород, запасы которых обнаружены на территории Западной Сибири [8].
Наличие болот и мелких рек, обогащенных гуминовыми веществами, предполагает присутствие в подземных водах органических веществ, что подтверждается аналитически. Так, значение перманганатной окисляемости подземных вод Западной Сибири составляет от 3 до 14 мг/л. В некоторых подземных водах, которые содержат железо в виде двухвалентного иона, при окислении в процессе водоподготовки образуются устойчивые коллоидные частицы [9; 10]. Их наличие обусловлено содержанием железа в виде Fe(OH)3, связанного с растворенными органическими веществами гумусового происхождения. Присутствие устойчивых коллоидных соединений железа является основной особенностью подземных вод Западно-Сибирского региона, которую необходимо учитывать при определении цветности с использованием методик, рекомендованных ГОСТ Р 52769-2007.
Для исследований были выбраны подземные воды Западно-Сибирского региона, отобранные с глубины 80–200 м. Эксперименты проводили как на месте отбора воды, так и в лабораторных условиях. Температура подземных вод на месте отбора составляла 279–284 К. Катионный и анионный состав этих вод определяли в соответствии с ГОСТ Р 51232-98, концентрации Fe (II) и Fe (III) – колориметрическим методом с о-фенантролином и сульфосалициловой кислотой соответственно. Полный анализ катионного состава примесей был получен с использованием плазменного оптического эмиссионного спектрометра ICP-OES фирмы «Varian» в Центре коллективного пользования Томского политехнического университета.
Органические вещества в воде определяли по значению перманганатной окисляемости, содержанию общего органического углерода и растворенного органического углерода на хроматографе ТОС-V фирмы «Shimadzu».
Распределение частиц по размерам было получено на анализаторе Zetasizer Nano ZS (Malvern Instruments). Размер частиц определялся по динамическому рассеянию света (угол рассеяния 173).
Регистрацию спектров оптического поглощения в диапазоне 200–500 нм проводили на спектрометре SPECORD M-40 фирмы «Carl Zeiss Jena». Значения рН и Eh определяли с помощью портативного анализатора воды Water Test фирмы «HANNA» (HI 98204).
Для фильтрации исследуемых вод использовали бумажные фильтры («синяя лента») с размером пор 3000–5000 нм и мембраны фирмы «Millipore» с размерами пор 200, 400, 450 и 1200 нм.
Цветность воды определяли на фотоколориметре КФК 2. При этом использовали синий светофильтр ( = 400 ± 5 нм с шириной полосы пропускания 45 ± 10 нм) и кюветы с размерами поглощающего слоя 5–10 см. Стандартные растворы готовили смешиванием известных количеств окрашенных солей двухромовокислого калия (К2Сг2О7) и сернокислого кобальта (CoSO4·7H2O).
Железосодержащие подземные воды по способности к образованию фильтруемых осадков при аэрации можно разделить на два типа [11; 12]. Первый тип – воды гидрокарбонатного состава, в которых железо находится в виде гидрокарбоната железа. Второй тип – воды, содержащие соединения железа, связанные с растворенными органическими веществами. В табл. 1 приведен химический состав подземных вод Западно-Сибирского региона первого ивторого типа.
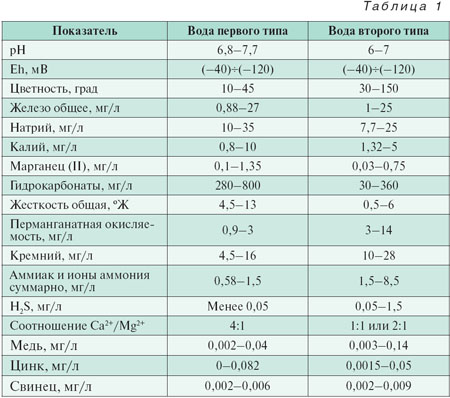
Наиболее характерными показателями воды первого типа являются соотношение концентраций ионов Са2+ и Mg2+ (примерно 4:1) и содержание гидрокарбонатов (280–800 мг/л). Количество органических веществ, определенных по значению перманганатной окисляемости, составляет 0,9–3 мг/л. После аэрации, отстаивания и фильтрования вода такого состава становится бесцветной, прозрачной и по качеству соответствует нормативным требованиям для питьевой воды.
Вода второго типа по сравнению с водой первого типа имеет более низкое значение рН, пониженное содержание солей жесткости и отличается большим значением перманганатной окисляемости, что указывает на присутствие в ней органических примесей. После аэрации, отстаивания и фильтрования вода такого состава остается желтоватого цвета, устойчивого во времени. Цвет воды обусловлен наличием коллоидных частиц, состоящих из Fe(OH)3, связанных с органическими веществами природного происхождения, обладающими защитными свойствами [13] и препятствующими коагуляции Fe(OH)3.
При использовании методики определения цветности подземных вод в соответствии с ГОСТ Р 52769-2007 возникают определенные трудности. Так, отбор проб рекомендуется производить в количестве 200 мл без консервации. Выполнять анализ следует как можно быстрее после отбора. Подземные воды как первого, так и второго типов имеют температуру 275–284 К, содержат железо только в виде Fe (II) и по визуальной оценке бесцветны лишь в первый момент после отбора пробы. При контакте с кислородом воздуха Fe (II) окисляется, образуя Fe(OH)3.
На рис. 1 представлены кинетические зависимости изменения концентрации Fe (III), образующегося в процессе аэрации подземных вод.
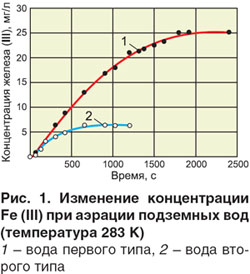
В водах первого типа после окисления Fe (II) цветность воды, обусловленная присутствием взвешенных частиц Fe(OH)3, в соответствии с РД 52.24.497-2005, характеризуется термином «кажущаяся» цветность. Как видно из рис. 1, концентрация Fe (III), а следовательно, и «кажущаяся» цветность воды возрастают со временем, достигая стационарного значения, которое характеризует полное окисление Fe (II). Последующее фильтрование воды на фильтре с размером пор 0,45 мкм, рекомендуемом ГОСТом, приводит к полному удалению Fe(OH)3.
В этом случае вода имеет «истинную» цветность, которая обусловлена только растворенными органическими веществами. Следует отметить, что окисление Fe (II) происходит и в процессе фильтрования исходной пробы. Ионы Fe (II) фильтром не задерживаются, и процесс окисления, продолжающийся после фильтрования, обусловливает ошибку при измерении «истинной» цветности. Определенная после полного окисления Fe (II) и последующего фильтрования «истинная» цветность подземных вод первого типа, как правило, соответствует нормативным значениям. Результаты, полученные на воде первого типа, приведены в табл. 2.
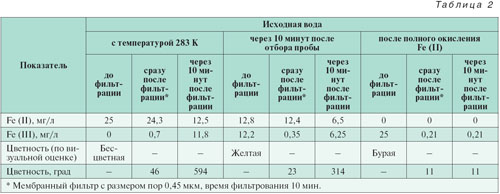
Из табл. 2 видно, что исходная вода прозрачна. В процессе окисления Fe (II) происходит увеличение концентрации Fe (III), которая характеризует «кажущуюся» цветность воды. Определение «истинной» цветности воды первого типа следует проводить после полного окисления Fe (II) с последующим фильтрованием. В этом случае такие показатели, как температура и время проведения анализа после отбора пробы не влияют на точность получаемых результатов.
В воде второго типа аналогичный процесс [полное окисление Fe (II) и последующее фильтрование через мембранный фильтр с диаметром пор 0,45 мкм] не приводит к полному удалению Fe(OH)3. В растворе остается гидроксид железа (III), связанный с органическими веществами в виде коллоидных частиц, придающих воде желтоватую окраску. На рис. 2 показана взаимосвязь «кажущейся» цветности воды второго типа с концентрацией Fe (III), оставшегося в фильтрате после использования фильтра с размером пор 0,45 мкм.
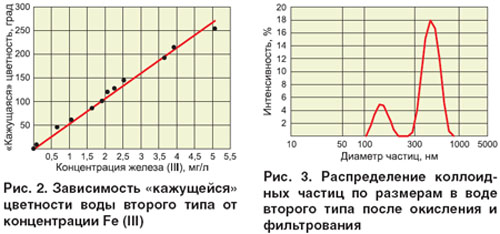
Для определения размера коллоидных частиц использовали воду второго типа с концентрацией Fe (III) 6,26 мг/л.
Для удаления частиц, способных образовывать осадок, исследуемую воду предварительно фильтровали через мембранный фильтр с размером пор 1200 нм. Распределение коллоидных частиц по размерам приведено на рис. 3, из которого видно, что в воде второго типа присутствуют два вида частиц, содержащих Fe(OH)3, связанных с растворенными органическими веществами. Частицы одного вида имеют размеры примерно от 110 до 270 нм и второго вида – размеры примерно от 300 до 800 нм. Таким образом, при фильтровании воды второго типа через мембранный фильтр с размером пор 0,45 мкм задерживаются не все коллоидные частицы.
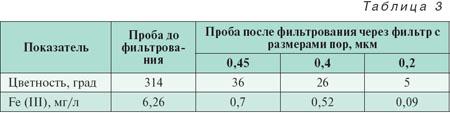
В табл. 3 приведены показатели воды второго типа [цветность и концентрация Fe (III)] до и после фильтрования на мембранных фильтрах фирмы «Millipore» с размером пор 0,45; 0,4; 0,2 мкм. Из табл. 3 видно, что при использовании мембранных фильтров с размером пор 0,45 мкм действительно не может быть установлена «истинная» цветность воды второго типа, которая достигается только после фильтрации через мембранные фильтры c размером пор 0,2 мкм. Таким образом, для подземных вод второго типа по методике, рекомендуемой ГОСТ Р 52769-2007, можно определить только «кажущуюся» цветность.
Выводы
Проведенные исследования подземных вод Западно-Сибирского региона показали неоднозначность результатов по определению цветности. Этот факт обусловлен особенностями химического состава воды. Наличие в подземных водах Fe (II) и его окисление при контакте с кислородом воздуха не позволяют проводить измерение цветности воды непосредственно после отбора пробы.
«Истинную» цветность воды, содержащей соединения железа, связанные с растворенными органическими веществами, можно измерять только после полного окисления Fe (II) и фильтрования через фильтр с размером пор 0,2 мкм. В этом случае температура и время проведения анализа после отбора пробы не влияют на точность получаемых результатов. В таких подземных водах присутствуют коллоидные частицы двух видов с максимальным распределением на 130 и 460 нм, обусловливающие цветность воды. Наличие этих частиц не позволяет определять «истинную» цветность, так как они не удаляются при фильтровании через фильтр с размером пор 0,45 мкм, рекомендованный ГОСТ. Поэтому целесообразно пользоваться только термином «кажущаяся» цветность.
Авторы благодарят сотрудников Технического университета г. Карлсруэ (Германия) и Центра коллективного пользования Томского политехнического университета за предоставленную возможность проведения серии экспериментов на их оборудовании.
Список литературы
- Кирюхин В. К., Мелькановицкая С. Г., Швец В. М. Определение органических веществ в подземных водах. – М.: Недра, 1976.
- Швец В. М. Органические вещества подземных вод. – М.: Недра, 1973.
- Труфанов А. И. Формирование железистых подземных вод. – М.: Наука, 1982.
- Унифицированные методы анализа вод: Под. ред. Ю. Ю. Лурье. – М.: Химия, 1973.
- Фомин Г. С. Вода. Контроль химической, бактериальной и радиационной безопасности по международным стандартам: Энциклопедический справ. – М.: Протектор, 1995.
- Зекцер И. С., Язвин Л. С. Ресурсы подземных вод и их использование / Водные проблемы на рубеже веков. – М.: Наука, 1999.
- О состоянии водных ресурсов Российской Федерации в 2002 году: Государственный доклад. – М.: НИА-Природа, 2003.
- Назаров А. Д., Шварцев С. Л. Подземные воды и их использование // Природные ресурсы Томской области. – Новосибирск: Наука, Сиб. отделение, 1991.
- Serikov L. V., Shiyan L. N., Tropina E. A. Oxidation of different forms of iron compositions in the underground water: 8th Korea-Russia Intern. Symp. on Science and Technology. 26 Jun. – 3 Jul. 2004. – Tomsk, 2004. V. II.
- Сериков Л. В., Шиян Л. Н., Тропина Е. А. и др. Коллоидные системы подземных вод Западно-Сибирского региона // Известия Томского политехнического университета. 2006. Т. 309. № 6.
- Яворовский Н. А., Сериков Л. В., Шиян Л. Н. и др. Особенности химического состава подземных источников Томской области. – Томск: Изд. дом «Цхай и К», 2005.
- Сериков Л. В., Шиян Л. Н., Тропина Е. А. Окисление различных форм соединений железа в скважинных водах / Высокоразбавленные системы: массоперенос, реакции и процессы: Матер. нем.-рус. семинара 15–17 октября 2005 г. – Томск, 2005.
- Воюцкий С. С. Курс коллоидной химии. – М.: Химия, 1976.







