№6|2011
ПИТЬЕВОЕ ВОДОСНАБЖЕНИЕ
bbk 000000
УДК 628162.1
Деманганация речной воды
Аннотация
Рассматривается одна из трудно решаемых проблем коммунальных сооружений очистки воды поверхностных источников – невозможность осуществления деманганации по классической схеме водоподготовки. Приведены результаты исследований по доочистке речной воды от марганца с помощью перманганата калия на сооружениях водоснабжения г. Пугачева Саратовской области. При выборе способа снижения содержания марганца учитывались водородный показатель и окислительно-восстановительный потенциал среды. Проведенные исследования и пробная эксплуатация системы дозирования перманганата калия показали, что обработка этим реагентом обеспечивает остаточное содержание марганца в питьевой воде, соответствующее нормативным требованиям.
Ключевые слова
питьевая вода , водоподготовка , марганец , водоисточник , перманганат калия , деманганация
Скачать статью в журнальной верстке (PDF)
В ряде регионов России специалисты все чаще отмечают многократное превышение фонового содержания марганца в воде малых рек [1–7]. В то же время данные по токсичности марганца [8] показывают, что деманганация питьевой воды – одно из значимых направлений водоподготовки.
Увеличение содержания растворимых форм марганца наблюдается в период ледостава, а также в летние месяцы (июль–август), когда вода источника прогревается до температуры выше 20 С. Обычно максимальная концентрация марганца фиксировалась к концу ледостава. Однако в последние годы в связи с климатическими изменениями (экстремально высокие летние температуры) эта тенденция нарушилась: в конце лета в водотоках наблюдается максимальное содержание марганца, в сотни раз превышащее фоновые значения. В конечном результате это сказывается на качестве воды, подаваемой потребителям, поскольку традиционные схемы водоподготовки (одно- и двухступенчатые, с применением коагулянта, флокулянта и хлорсодержащих реагентов) не обеспечивают снижение содержания марганца до нормативного значения.
Типичная ситуация имела место в г. Пугачеве Саратовской области летом 2009 г., когда в течение длительного времени сохранялась аномально высокая температура воздуха и, как следствие, воды поверхностного источника водоснабжения [9]. Для хозяйственно-питьевого водоснабжения города используется вода Сулакского водохранилища, расположенного на 186-м километре реки Большой Иргиз. Река протекает на территории Ивантеевского, Пугачевского, Балаковского районов и является левобережным притоком реки Волги (Волгоградское водохранилище).
В результате исследования проб воды в конце июля 2009 г. в водоисточнике был обнаружен марганец в концентрации 2,6–3,5 мг/л (обычно его фоновое содержание не превышает 0,05 мг/л). Водозаборно-очистные сооружения (ВОС) г. Пугачева построены в 1983 г. по проекту ЦНИИЭП инженерного оборудования и предназначены для очистки поверхностных вод до нормативного качества по мутности и цветности. Технология предусматривает забор воды из водоисточника, первичное хлорирование, обработку коагулянтом («АКВА-АУРАТ™30»), осветление на контактных осветлителях, вторичное хлорирование и подачу потребителям. Эффективность удаления марганца на ВОС составила 7–8%.
В связи с чрезвычайным характером ситуации срочно потребовалось проведение комплекса технологических работ для доочистки воды от марганца на ВОС г. Пугачева. Как правило, содержание марганца в речных водах составляет от сотых долей мкг/л до десятков мкг/л, в донных осадках – сотни мкг/кг. Марганец, поступающий в природные воды со стоком или из восстановительного горизонта водных отложений, не рассеивается, а сравнительно быстро окисляется и концентрируется в донных отложениях: на незначительных глубинах в зоне полного насыщения воды растворенным кислородом при рН 7,8–8,5 содержание растворенных форм марганца составляет десятые–сотые доли мг/л; восстановленные формы металлов сосредоточены в основном в глубоководной толще, поровых водах, в донных отложениях, где рН составляет 6,7–6,9, а содержание в воде кислорода 0,1–1,5 мг/л [10].
Перераспределение присутствующих в воде форм марганца (неорганические и органические комплексы, хелатированные формы, свободные ионы с молекулами воды в их первом координационном слое) зависит от значений водородного показателя рН и окислительно-восстановительного потенциала Eh среды. Эти основные показатели и используются при выборе способа очистки воды от марганца.
Известная диаграмма Пурбе Eh = f(pH) отражает состояние системы «марганец – вода» в координатах Eh–рН и дает наглядное представление о возможных способах очистки воды от марганца [11]. Как следует из диаграммы, для достоверной очистки воды от растворенных соединений марганца (II) должно выполняться условие рН > 8. При этом учитываются следующие факторы:
- повышение окислительно-восстановительного потенциала среды с помощью сильных окислителей без корректировки рН воды;
- повышение рН воды при недостаточном окислительно-восстановительном потенциале в случае использования слабых окислителей;
- применение более сильного окислителя с повышением рН воды.
С учетом возможности быстрой реализации технологии доочистки от марганца в условиях ВОС г. Пугачева было предложено использовать в качестве дополнительного реагента перманганат калия, который позволяет быстро и эффективно окислять Mn (II) до нерастворимого гидрата диоксида. Образующийся дисперсный осадок MnO2·2H2O или MnО(OH)2 имеет большую удельную поверхность и является эффективным сорбентом:
3Mn2+ + 2KMnO4 + 7H2O
5MnО(OН)2 + 4H+ + 2K+.
На окисление 1 мг Mn (II) расходуется 2,07 мг KMnO4 [12]. Для повышения эффективности процесса необходимо подщелачивание воды до рН > 8. Удаление марганца из поверхностных вод может осуществляться на фильтровальных станциях совместно с другими методами очистки воды (коагулирование, фильтрование, хлорирование). Эффективность очистки составляет 95–99%.
На первом этапе исследований была выполнена работа по уточнению состава речной воды, поступающей на ВОС. Результаты сокращенного технологического анализа приведены в таблице.
Определение температуры, рН и окислительно-восстановительного потенциала воды проводилось в проточных условиях с использованием ячейки специальной конструкции. Измерения осуществлялись прибором HANNA 8314 (Германия). Анализ содержания железа, марганца и сероводорода выполнялся спектрофотометрическим методом на приборе NOVA 60А («Merck», Германия). Методики анализа аттестованы в Российской Федерации, а приборы зарегистрированы в реестре Росстандарта.
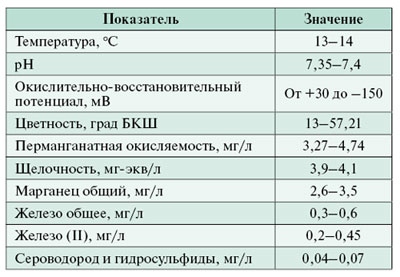
Результаты исследований показали, что на отметке приемного оголовка водозаборных сооружений выражены восстановительные условия среды (низкое значение окислительно-восстановительного потенциала, наличие сероводорода и двухвалентного железа), не свойственные природным условиям поверхностного водоема. В таких случаях отсутствует растворенный кислород, и в экосистеме в основном протекают процессы анаэробного характера.
Низкое значение водородного показателя позволяет предположить присутствие соединений марганца преимущественно в растворенном состоянии (с валентностью +2). Фильтрование проб речной воды через фильтр «синяя лента» показало, что массовое содержание нерастворенных соединений марганца находится в пределах 7–13% от общего его содержания. Для определения оптимальных условий деманганации на втором этапе исследований изучался процесс подщелачивания речной воды. В качестве реагента использовалась каустическая сода высокой чистоты [13].
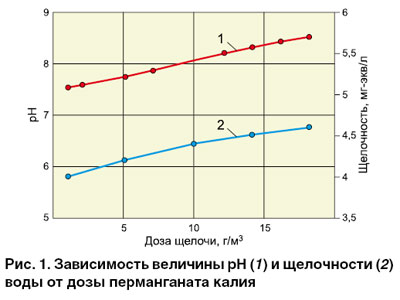
На рис. 1 представлена зависимость величины рН и щелочности воды от дозы реагента. Для достижения оптимального для окисления марганца значения pH (более 8) требуется около 10 г/м3 щелочи, при этом природная щелочность воды возрастает на 10%. Процесс деманганации (как и подщелачивания) изучали в условиях свободного объема. В качестве реакционного сосуда использовался стакан объемом 1 л, размещенный на магнитной мешалке. Отделение продуктов реакции проводилось фильтрованием (фильтр «синяя лента»).
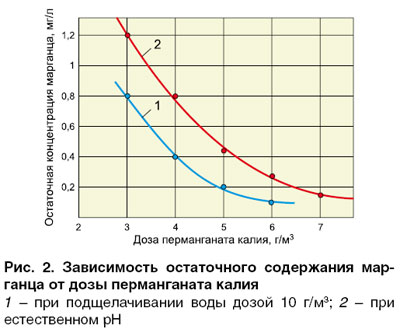
Применяемый в опытах перманганат калия квалифицирован как «реагент питьевого водоснабжения» [14]. На рис. 2 представлена зависимость величины остаточного содержания марганца от дозы перманганата калия при естественном рН речной воды и при подщелачивании (рН 8). Для достижения нормативной величины остаточного содержания марганца (0,1 мг/л) без подщелачивания необходима доза реагента 8 г/м3, при подщелачивании – 6 г/м3.
Следует обратить внимание, что кинетика окисления марганца в щелочной среде практически совпадает со стехиометрией реакции окисления двухвалентного марганца перманганатом калия. Это косвенно подтверждает наличие в речной воде преимущественно растворенных соединений марганца (+2). При подщелачивании быстро образуются крупные хлопья гидроокиси, легко отделяемые фильтрованием. При обработке окислителем без подщелачивания образуется мелкая, медленно фильтрующаяся взвесь.
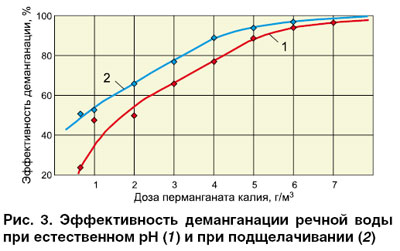
Таким образом, деманганация исследуемой речной воды перманганатом калия может быть обеспечена даже без применения щелочных реагентов. При этом необходимо использовать качественный загрузочный материал при низкой скорости фильтрования. На рис. 3 представлена зависимость эффективности деманганации от дозы перманганата калия при естественном рН и при подщелачивании исходной воды. Эффективность процесса составила не менее 97%. Обработка речной воды перманганатом калия обеспечивает также высокое качество фильтрата по следующим показателям: запах, привкус, содержание общего железа и сероводорода. При реализации процесса деманганации с подщелачиванием для упрощения технологической схемы может использоваться комбинированный реагент – щелочной раствор перманганата калия.
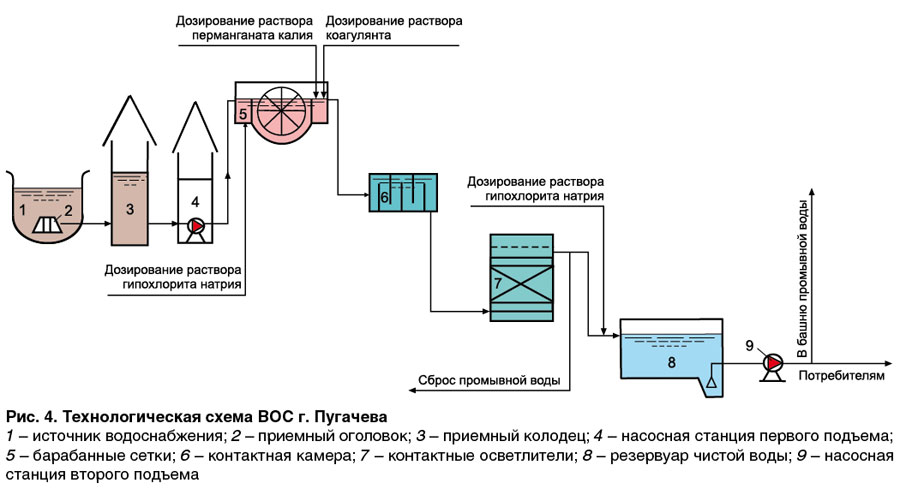
На основании полученных результатов исследований на ВОС г. Пугачева было организовано дозирование перманганата калия путем свободного излива из емкости приготовленного раствора в приемный карман одной из барабанных сеток (рис. 4). Для приготовления раствора с концентрацией около 1,5% использовалась вода естественной температуры с барботажем воздухом.
Пробная эксплуатация системы дозирования перманганата калия показала возможность полного окисления марганца в речной воде – его остаточное содержание после контактной камеры не превышало 0,1 мг/л. Однако полное отделение продуктов реакции на контактных осветлителях вызвало затруднения из-за низкого качества загрузочного материала. После замены загрузки очистные сооружения способны обеспечить нормативное качество очищенной воды по содержанию марганца при его сезонных колебаниях в водоисточнике. При этом первичное хлорирование не влияет на процесс деманганации воды, а последующая коагуляция позволит улучшить отделение продуктов реакции.
Следует также отметить, что с появлением на рынке перманганата калия, выпускаемого по международному стандарту ANSI/AWWA B 603-93, на станциях водоподготовки с самотечной схемой деманганация может осуществляться весьма оперативно – путем организации систем сухого дозирования. Возможность этого варианта определяется техническими характеристиками реагента.
Выводы
Необходимость соблюдения гигиенического норматива по содержанию марганца в питьевой воде в совокупности с данными по его токсичности позволяют считать деманганацию одним из значимых направлений водоподготовки. Эффективное удаление марганца из поверхностных вод обработкой перманганатом калия может осуществляться на фильтровальных станциях совместно с другими методами очистки воды (коагулированием, фильтрованием, хлорированием). Проведенные исследования и пробная эксплуатация системы дозирования показали, что обработка перманганатом калия обеспечивает остаточное содержание марганца в питьевой воде, соответствующее нормативным требованиям.
Список цитируемой литературы
- Государственный доклад о состоянии окружающей среды и влиянии факторов среды обитания на здоровье населения Свердловской области в 2009 году. – Екатеринбург, 2010.
- Экологическая обстановка на территории Самарской области в 2009 году. Пресс-релиз по данным государственного мониторинга Приволжского УГМС. – Самара, Министерство природных ресурсов и экологии РФ, 2010.
- Экологический бюллетень. Ноябрь 2010 г. – Самара, Министерство природных ресурсов и экологии РФ, 2010.
- Экологический бюллетень. Апрель 2010 г. – Самара, Министерство природных ресурсов и экологии РФ, 2010.
- Степанцов А. Казанка утекла из города / http://116.ru/news/317286.html.
- VIII Международный симпозиум «Чистая вода России – 2005»: Тез. докл. – Екатеринбург, 2005.
- Морозов С. В., Кузубова Л. И. Марганец в питьевой воде: Аналитический обзор. – Новосибирск, 1991.
- Бочаров В. Л., Бугреева М. Н., Смирнова А. Я. Экологическая геохимия марганца. – Воронеж: Изд-во Воронежского университета, 1998.
- Фрог Б. Н., Левченко А. П. Водоподготовка. – М.: Изд-во МГУ, 1996.
- Шевченко М. А. и др. Окислители в технологии водообработки. – Киев: Наукова думка, 1979.
- Санитарно-эпидемиологическое заключение 77.99.03.369.Д.011082.09.09 от 23 сентября 2009 г. Реагент питьевого водоснабжения «Ионная гранулированная гидроокись натрия (сода каустическая)».
- Санитарно-эпидемиологическое заключение 77.99.27.214.Д.000742.02.08 от 4 февраля 2008 г. Реагент питьевого водоснабжения «Перманганат калия (калий марганцовокислый) модифицированный».